



25 مارس 2024 - در سلولهای عصبی، هورمون انسولین تنظیم میکند که آیا میتوکندریها بازیافت شوند یا به کار خود پیدا دهند.
هورمون انسولین بسیاری از فرآیندهای سلولی را کنترل می کند و آنها را با ذخیره ی انرژی فعلی بدن سازگار می کند. آنجلیکا هاربائر و تیمش از موسسه ی هوش بیولوژیکی ماکس پلانک کشف کردند که یکی از فرآیندهای تنظیم شده توسط انسولین، کنترل کیفیت نیروگاه های سلولی در سلول های عصبی است. هنگامی که انرژی کافی در بدن در دسترس باشد، انسولین از بین بردن میتوکندری های معیوب را تسهیل می کند. هنگامی که انرژی کمیاب است یا سیگنال انسولین قطع می شود، بازیافت میتوکندری کاهش می یابد و سلول ها به استفاده از نیروگاه های قدیمی خود، حتی نیروگاه های بالقوه آسیب دیده ادامه می دهند. ادامه عملکرد میتوکندری های معیوب می تواند فرآیندهای پیری و بیماری های عصبی را تحت تاثیر قرار دهد.
سلول های عصبی برای تامین انرژی خود نیازهای ویژه ای دارند. به دلیل منشعب شدن گسترده و نیازهای بالای انرژی، آنها نیروگاه های سلولی خود، یعنی میتوکندری ها را زیر نظر دارند. سلول های عصبی باید اطمینان حاصل کنند که همیشه میتوکندری های کافی در امتداد آکسون ها وجود دارد، جایی که نیروگاه ها ارتباطات سلول با سلول های همسایه اش را تامین می کنند. به همین دلیل است که نورونها میتوکندریها را حتی به دورافتادهترین نقاط سلولیشان منتقل میکنند.
تحقیقات قبلی آنجلیکا هاربائر نشان داده بود که میتوکندری ها نقشه های پروتئین PINK1 را در سفر خود درون نورون به همراه دارند. دکتر هاربائر، سرپرست گروه تحقیقاتی ماکس پلانک توضیح داد: PINK1، یک پروتئین کلیدی است که زمانی عمل میکند که میتوکندریها باید حذف شوند، زیرا دیگر به درستی کار نمیکنند. این پروتئین می تواند میتوکندری را برای بازیافت علامت گذاری کند و دقیقاً توسط سلول ها کنترل می شود. عدم کنترل PINK1 می تواند منجر به کمبود میتوکندری شود، در حالی که ادامه کار نیروگاه های سلولی معیوب می تواند به سلول آسیب برساند.
هورمونی با نقش های متعدد
آنجلیکا هاربائر و تیمش اکنون کشف کردند که هورمون انسولین در کنترل کیفیت میتوکندری در نورون ها نقش دارد. انسولین برای نقشش در تنظیم جذب قند توسط سلول ها معروف و شناخته شده است. همچنین بسیاری از فرآیندهای درون سلول ها را کنترل می کند تا دقیقاً آنها را با ذخیره ی انرژی فعلی بدن تنظیم کند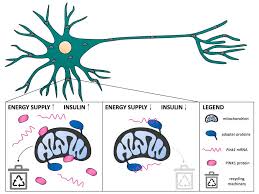 .
.
در مورد بازیافت میتوکندری، این کار به شرح زیر است: در میتوکندری، نقشه های PINK1 به عنوان مولکول های mRNA ذخیره می شوند. اگر انرژی کافی در دسترس باشد، سیگنالی از گیرنده ی انسولین در سطح سلول به میتوکندری منتقل می شود. هنگامی که سیگنال انسولین می رسد، نقشه ها توسط میتوکندری آزاد می شوند و سلول می تواند پروتئین PINK1 اضافی تولید کند. این تضمین می کند که میتوکندری های معیوب به طور موثر حذف می شوند. در صورت کمبود انرژی، یا اگر سیگنال گیرنده انسولین از دست رفته باشد، بلوپرینت ها یا نقشه های PINK1 به شدت به میتوکندری متصل می شوند.
از یک طرف، اتصال محکم به میتوکندری به طرحهای PINK1 اجازه میدهد تا در امتداد رشته ی طولانی سلولهای عصبی(اکسون) حرکت کنند. از سوی دیگر، در دسترس بودن مولکولهای mRNA برای تولید PINK1 را کاهش میدهد. سطح پروتئین PINK1 پایین باقی می ماند و بازیافت میتوکندری کاهش می یابد- حتی اگر این امر سبب ادامه کار نیروگاه های آسیب دیده شود.
تابیتا هیس، نویسنده ی ارشد این مطالعه، گفت: ما انتظار داشتیم که اتصال mRNA به میتوکندری باعث افزایش تولید PINK1 شود. با کمال تعجب، آزمایشهای ما نشان داد که اینطور نیست. وقتی سطح انرژی پایین است، ظاهراً برای سلولها بهتر است که پروتئین PINK1 کمتری تولید کنند و به استفاده از میتوکندریهای بالقوه آسیبدیده ادامه دهند.
قطع سیگنال دهی انسولین با پیامدهایی برای بیماری و پیری مرتبط است
هنگامی که انتقال سیگنال از گیرنده انسولین به میتوکندری به دلیل بیماری مختل می شود، وضعیت مشابهی ممکن است رخ دهد. سیگنالدهی ناقص انسولین یکی از مشخصههای دیابت است و در بیماری آلزایمر نیز در مغز مشاهده شده است. همچنین مشخص شده است که کنترل ناکارآمد کیفیت میتوکندری میتواند به بیماریهای نورودژنراتیو مختلف منجر شود. دکتر هاربائر گفت: مشاهدات ما به درک ما از چگونگی ارتباط بین تأمین انرژی سلولی، پیری و بیماریهای عصبی کمک نمود.
در مرحله بعد، محققان قصد دارند بررسی کنند که پس از رها شدن از میتوکندری به داخل سلول چه اتفاقی برای نقشه های PINK1 می افتد. دکتر تابیتا هیس گفت: ما بهویژه علاقهمندیم که بفهمیم پروتئینPINK1 در کجا ساخته میشود، اگر در میتوکندری ساخته نمی شود، چگونه پس از تولید راه خود را به میتوکندری پیدا میکند. تنها زمانی که این دو مرحله ادامه یابند،PINK1 بازیافت نیروگاه های معیوب را برای جلوگیری از آسیب رساندن به سلول عصبی آغاز می کند.
منبع:
https://www.sciencedaily.com/releases/2024/03/240319123020.htm